La matière et ses états
Problématique — Comment reconnaître et comprendre les différents états de la matière que nous rencontrons au quotidien ?
Comment reconnaître et comprendre les différents états de la matière que nous rencontrons au quotidien ?
- Connaître les trois états principaux de la matière : solide, liquide et gaz.
- Savoir décrire les caractéristiques de chaque état.
- Comprendre les principaux changements d’état de la matière.
Partie 1 : Qu’est-ce que la matière ?
La matière est tout ce qui occupe de la place et possède une masse. Autour de nous, presque tout est fait de matière : l’eau, l’air, les roches, les objets, les aliments ou encore notre corps. Même lorsque l’on ne la voit pas bien, comme dans le cas de l’air, la matière est bien présente.
La matière peut exister sous différentes formes appelées états.
Pour expliquer le comportement de la matière, on utilise souvent un modèle simple : on imagine qu’elle est constituée de très petites particules. Ce modèle aide à comprendre pourquoi un solide garde sa forme, pourquoi un liquide s’écoule et pourquoi un gaz occupe tout l’espace disponible.
La matière est présente partout dans notre environnement. Elle occupe un volume et possède une masse, même lorsqu’elle est difficile à voir, comme l’air. Pour mieux comprendre son comportement, on utilise un modèle dans lequel la matière est formée de très petites particules. Ce modèle permet ensuite d’expliquer les différents états de la matière et leurs propriétés.
Partie 2 : Les trois états de la matière
L’état solide
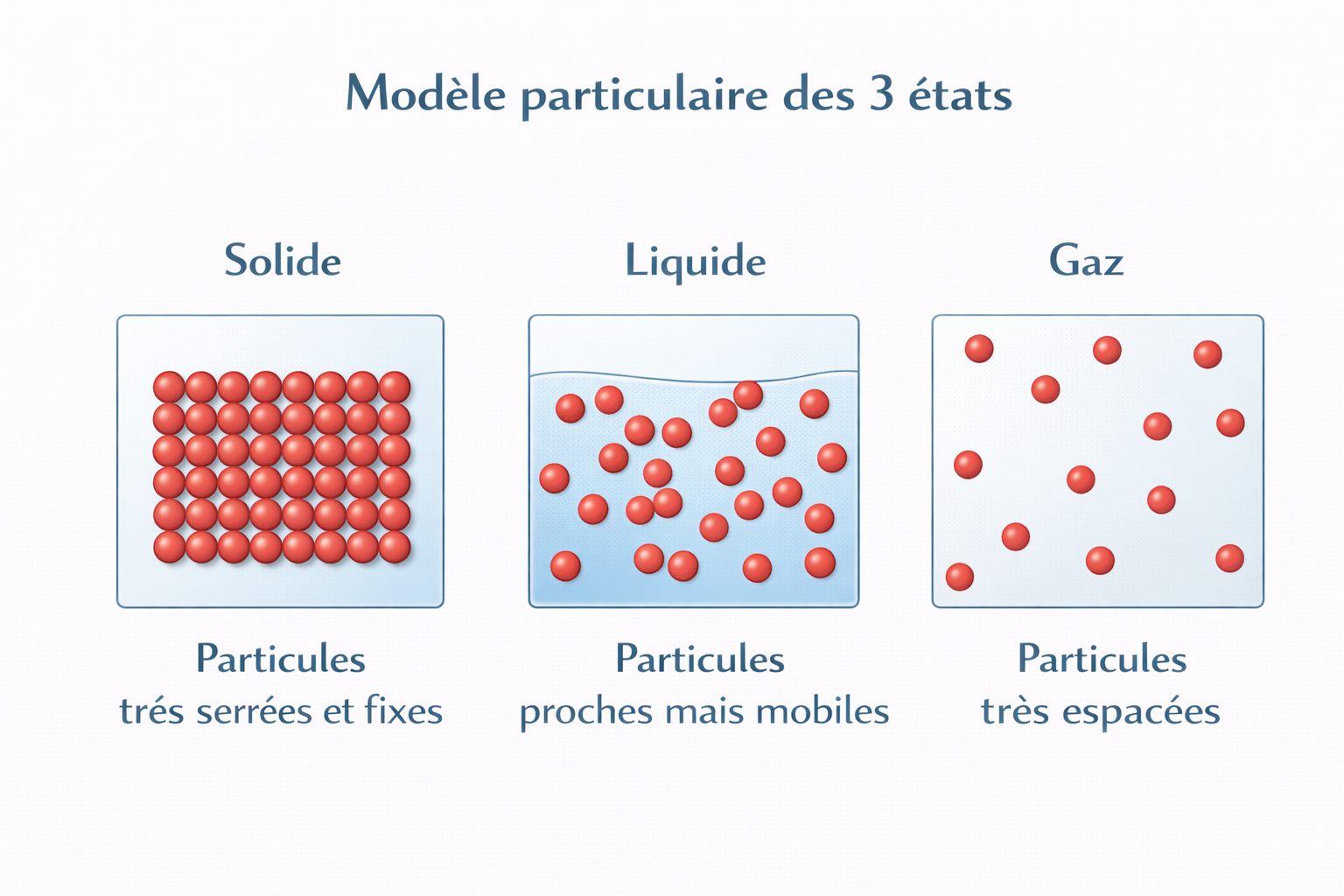
Un solide possède une forme propre et un volume propre. Cela signifie qu’il garde sa forme même si on le change de récipient. Dans le modèle particulaire, les particules sont très proches les unes des autres et ne font que vibrer autour de leur place. Exemples : un glaçon, une pierre, une gomme.
L’état liquide
Un liquide possède un volume propre mais pas de forme propre. Il prend la forme du récipient qui le contient. Dans le modèle particulaire, les particules restent proches, mais elles peuvent se déplacer les unes par rapport aux autres. Exemples : l’eau, le lait, le jus de fruit.
L’état gazeux
Un gaz n’a ni forme propre ni volume propre. Il se répand dans tout l’espace disponible. Dans le modèle particulaire, les particules sont très espacées et se déplacent dans tous les sens. Exemples : l’air, le dioxygène, la vapeur d’eau.
La vapeur d’eau est un gaz invisible. Le “nuage blanc” que l’on voit au-dessus d’une casserole ne correspond pas à la vapeur d’eau elle-même, mais à de très fines gouttelettes d’eau liquide formées lorsque la vapeur se refroidit.
| État | Forme / Volume | Disposition des particules | Exemples |
|---|---|---|---|
| Solide | Forme et volume propres | Très proches, vibrent sans se déplacer librement | Glaçon, pierre |
| Liquide | Pas de forme propre, volume propre | Proches, peuvent glisser les unes sur les autres | Eau, jus de fruit |
| Gazeux | Ni forme propre ni volume propre | Très espacées, se déplacent librement | Air, vapeur d’eau |
Les trois états de la matière se distinguent par leur forme, leur volume et la manière dont on représente les particules. Un solide garde sa forme et son volume, un liquide garde son volume mais prend la forme du récipient, et un gaz n’a ni forme propre ni volume propre. Ces différences permettent de reconnaître facilement l’état d’une matière dans la vie quotidienne et d’expliquer son comportement.
Partie 3 : Les changements d’état
La matière peut passer d’un état à un autre lorsqu’elle gagne ou perd de l’énergie thermique, le plus souvent lorsqu’on la chauffe ou qu’on la refroidit. Ces transformations s’appellent des changements d’état.
- Fusion : solide → liquide (ex. : glace qui fond).
- Solidification : liquide → solide (ex. : eau qui gèle).
- Vaporisation : liquide → gaz (ex. : eau qui bout ou eau qui s’évapore).
- Liquéfaction : gaz → liquide (ex. : formation de buée sur une vitre froide).
L’évaporation est une forme de vaporisation lente qui se produit à la surface d’un liquide, sans qu’il soit nécessaire d’atteindre l’ébullition. Par exemple, une flaque d’eau peut disparaître peu à peu.
| Changement | De → Vers | Exemple |
|---|---|---|
| Fusion | Solide → Liquide | Glace qui fond |
| Solidification | Liquide → Solide | Eau qui gèle |
| Vaporisation | Liquide → Gaz | Eau qui bout / évaporation |
| Liquéfaction | Gaz → Liquide | Buée sur une vitre |
Il existe aussi d’autres changements d’état, comme la sublimation (solide → gaz) et la condensation solide ou dépôt (gaz → solide). Par exemple, le givre peut se former directement à partir de la vapeur d’eau présente dans l’air.
La matière peut changer d’état sans changer de nature. Par exemple, l’eau peut être solide, liquide ou gazeuse tout en restant de l’eau. Les changements d’état dépendent surtout de la température, et parfois aussi d’autres conditions comme la pression. Ils sont souvent réversibles : une glace peut fondre, puis l’eau obtenue peut de nouveau geler. Comprendre ces transformations permet d’expliquer de nombreux phénomènes observés dans la nature et dans la vie quotidienne.
La matière existe principalement sous trois états : solide, liquide et gazeux. Chaque état possède des caractéristiques particulières de forme, de volume et d’organisation des particules. La matière peut passer d’un état à un autre lorsqu’elle est chauffée ou refroidie : ce sont les changements d’état. Ces transformations expliquent de nombreux phénomènes quotidiens, comme la glace qui fond, l’eau qui s’évapore ou la buée qui apparaît sur une vitre. Comprendre les états de la matière est une base importante pour mieux étudier les sciences physiques et chimiques au collège.