Énergie et transformations chimiques
Problématique — Comment l’énergie intervient-elle lors des transformations chimiques ?
Comment l’énergie intervient-elle lors des transformations chimiques ?
- Comprendre que les réactions chimiques s’accompagnent d’échanges d’énergie.
- Identifier les réactions exothermiques et endothermiques.
- Savoir que l’énergie peut se présenter sous différentes formes (chaleur, lumière, électricité...).
- Comprendre qu’une réaction peut nécessiter une énergie de démarrage (énergie d’activation).
Partie 1 : L’énergie dans les réactions chimiques
Lors d’une transformation chimique, des liaisons entre atomes se cassent et d’autres se forment. Casser des liaisons consomme de l’énergie, tandis que former des liaisons libère de l’énergie.
L’énergie est une grandeur qui mesure la capacité d’un système à provoquer une transformation (échanger de la chaleur, fournir un travail, émettre de la lumière...).
| Étape | Effet sur l’énergie |
|---|---|
| Cassure de liaisons | Nécessite de l’énergie |
| Formation de liaisons | Libère de l’énergie |
Le bilan énergétique d’une réaction dépend de la comparaison entre l’énergie consommée pour casser les liaisons et l’énergie libérée lors de la formation de nouvelles liaisons.
- Les réactions chimiques impliquent toujours des échanges d’énergie.
- Casser des liaisons consomme de l’énergie, former des liaisons en libère.
Partie 2 : Réactions exothermiques et endothermiques
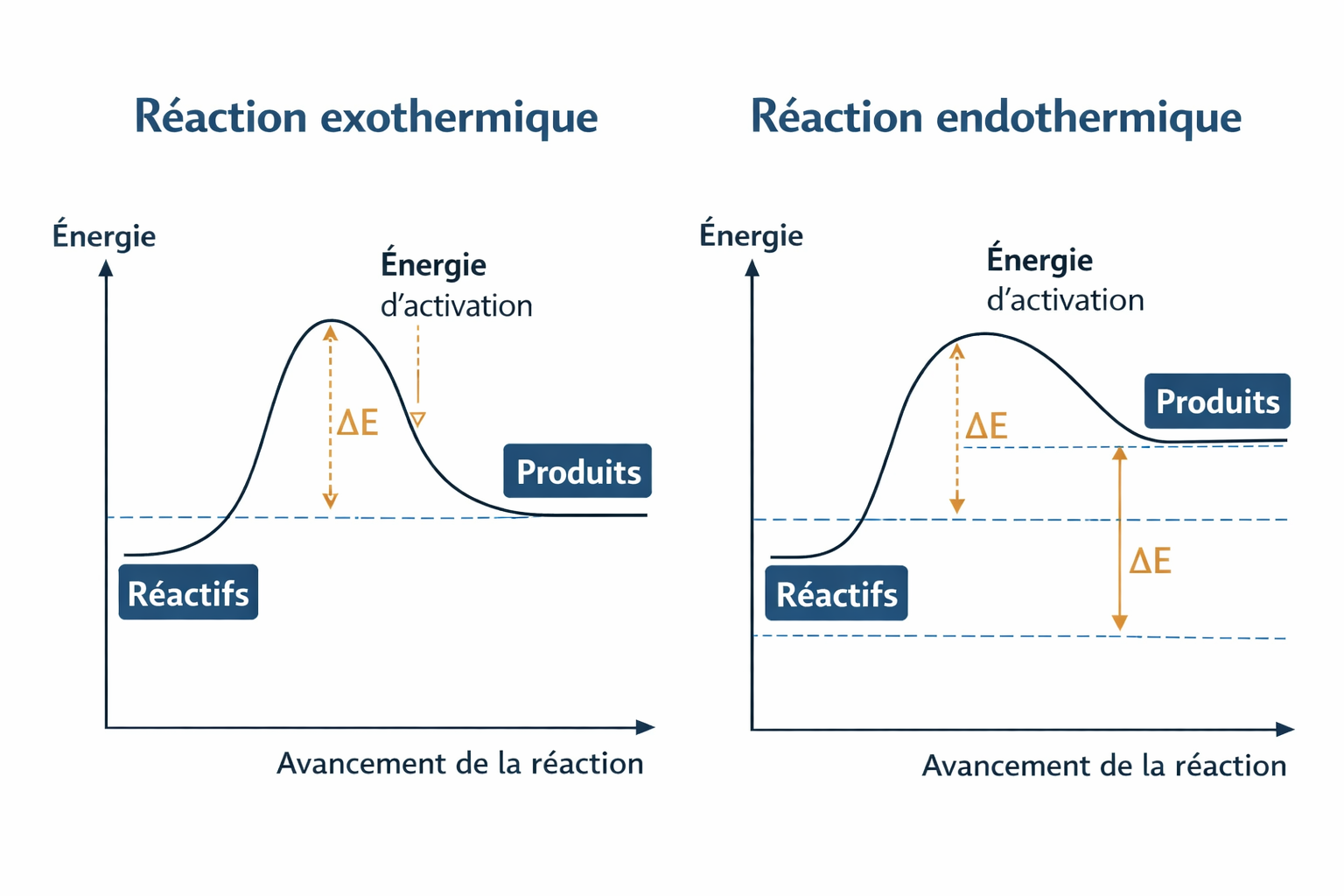
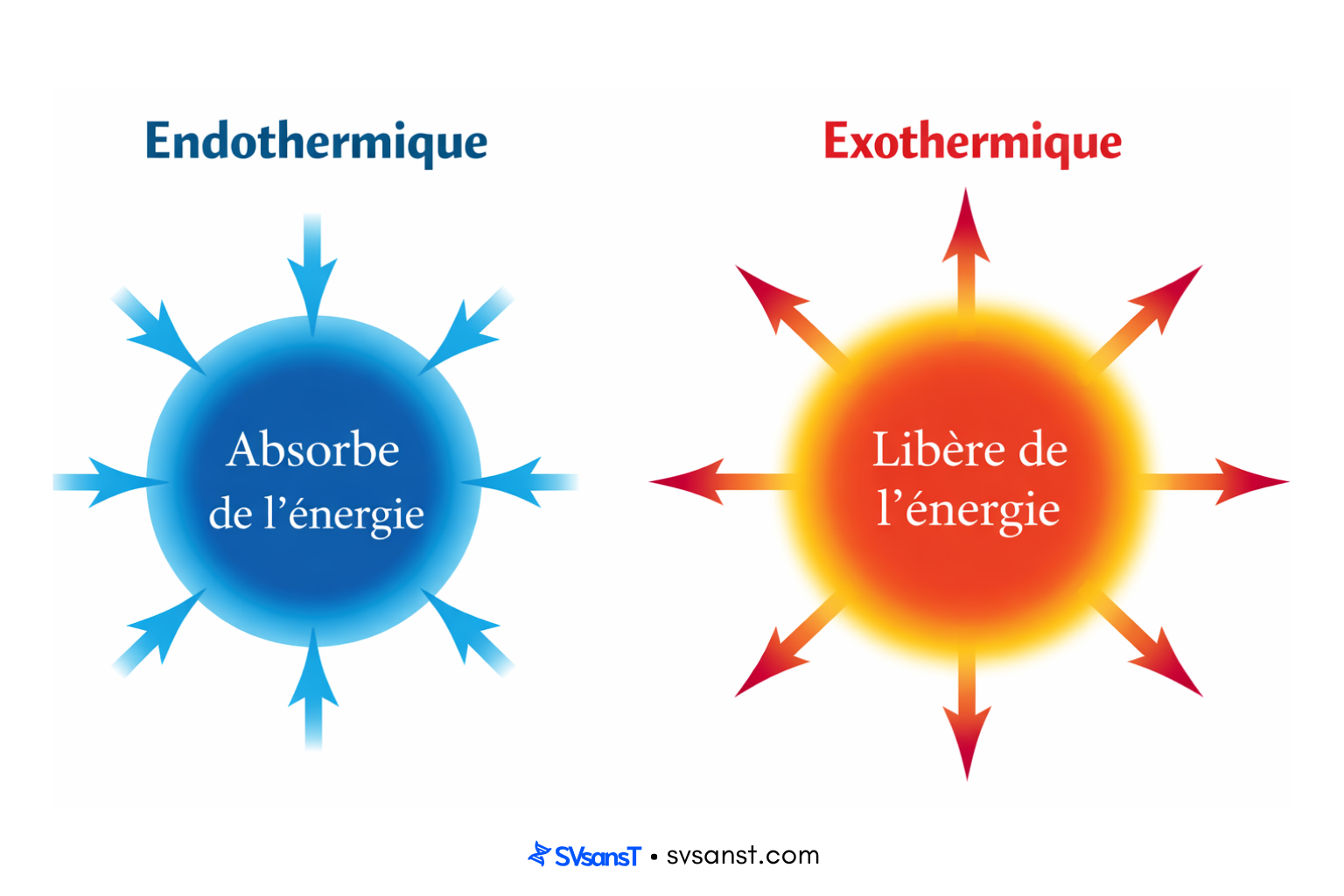
Réaction exothermique : libère de l’énergie vers le milieu extérieur (souvent sous forme de chaleur, parfois aussi de lumière). Exemple : combustion.
Réaction endothermique : absorbe de l’énergie pour se produire. Exemple : photosynthèse, qui nécessite de l’énergie lumineuse.
| Type de réaction | Échange d’énergie | Indice fréquent | Exemple |
|---|---|---|---|
| Exothermique | Libération d’énergie (chaleur, lumière...) | Température du milieu augmente souvent | Combustion |
| Endothermique | Absorption d’énergie | Température du milieu baisse souvent | Photosynthèse (énergie lumineuse) |
Même une réaction exothermique peut avoir besoin d’un « coup de pouce » au départ : c’est l’énergie d’activation (par exemple, une étincelle pour démarrer une combustion).
- Exothermique : énergie libérée vers l’extérieur.
- Endothermique : énergie absorbée depuis l’extérieur.
- Une réaction peut nécessiter une énergie d’activation pour démarrer.
Partie 3 : Formes d’énergie dans les transformations chimiques
L’énergie échangée lors d’une réaction peut se manifester sous forme de chaleur, de lumière, de son ou d’énergie électrique.
La mesure de la température permet souvent de repérer un échange d’énergie thermique (mais ce n’est pas le seul signe possible).
| Forme d’énergie | Comment l’observer ? |
|---|---|
| Chaleur | Variation de température |
| Lumière | Émission lumineuse |
| Son | Bruit (détonation, crépitement...) |
| Électrique | Courant/tension produits ou consommés |
- L’énergie échangée peut prendre plusieurs formes : thermique, lumineuse, sonore, électrique.
- Une variation de température est un indice fréquent, mais pas unique.
Les transformations chimiques s’accompagnent toujours d’échanges d’énergie : certaines réactions libèrent de l’énergie (exothermiques), d’autres en absorbent (endothermiques). L’énergie peut apparaître sous différentes formes (chaleur, lumière, électricité...). Même une réaction exothermique peut nécessiter une énergie d’activation pour démarrer.