Mélanges et solutions
Problématique — Qu’est-ce qu’un mélange ? Comment distinguer un mélange d’une solution ? Comment peut-on séparer les composants d’un mélange ?
- Comprendre ce qu’est un mélange et une solution.
- Identifier les différents types de mélanges.
- Découvrir les méthodes pour séparer les composants d’un mélange.
- Comprendre l’importance de la dissolution dans la formation d’une solution.
Partie 1 : Qu’est-ce qu’un mélange ?
Un mélange est constitué de plusieurs substances mélangées ensemble sans réaction chimique. Chaque substance conserve ses propriétés.
Un mélange contient au moins deux substances différentes, visibles ou non, qui peuvent être séparées par des méthodes physiques.
- Eau + sable : mélange dont on distingue les constituants.
- Eau salée : mélange où le sel est dissous dans l’eau.
- Un mélange regroupe plusieurs substances qui coexistent sans se transformer chimiquement.
Partie 2 : Mélanges homogènes et hétérogènes
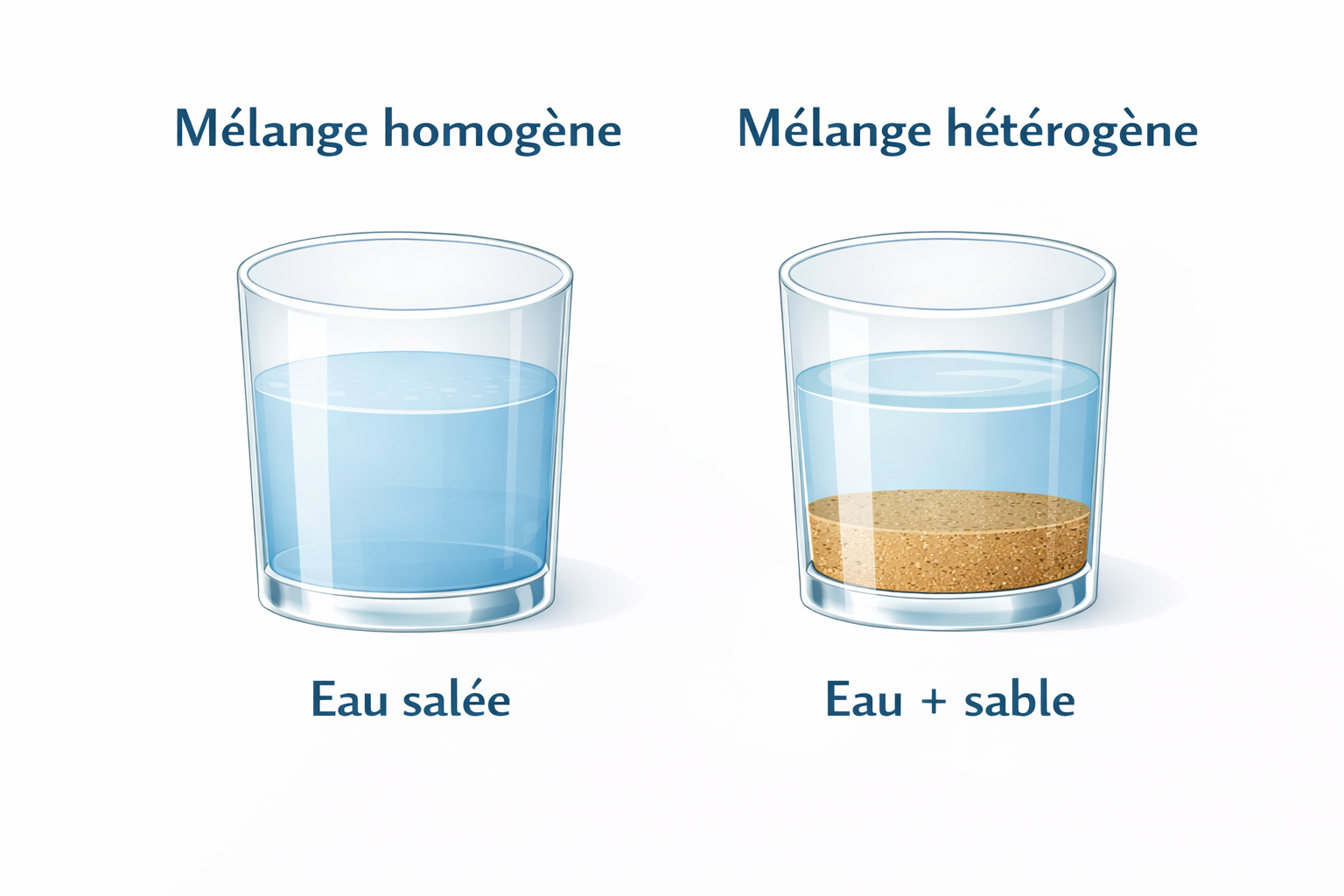
Mélange homogène
Les substances sont uniformément réparties : on ne distingue pas les composants à l’œil nu. Exemples : eau salée, air.
Mélange hétérogène
On peut distinguer les différentes substances : on observe plusieurs phases. Exemples : eau et sable, huile et eau.
| Type de mélange | Description | Exemple |
|---|---|---|
| Homogène | Substances uniformément réparties (aspect unique) | Eau salée, air |
| Hétérogène | Plusieurs phases visibles | Eau et sable, huile et eau |
- Les mélanges peuvent être homogènes ou hétérogènes selon la répartition des substances.
Partie 3 : La dissolution et la solution
La dissolution
La dissolution est le processus par lequel une substance (le soluté) se dissout dans un liquide (le solvant) pour former une solution.
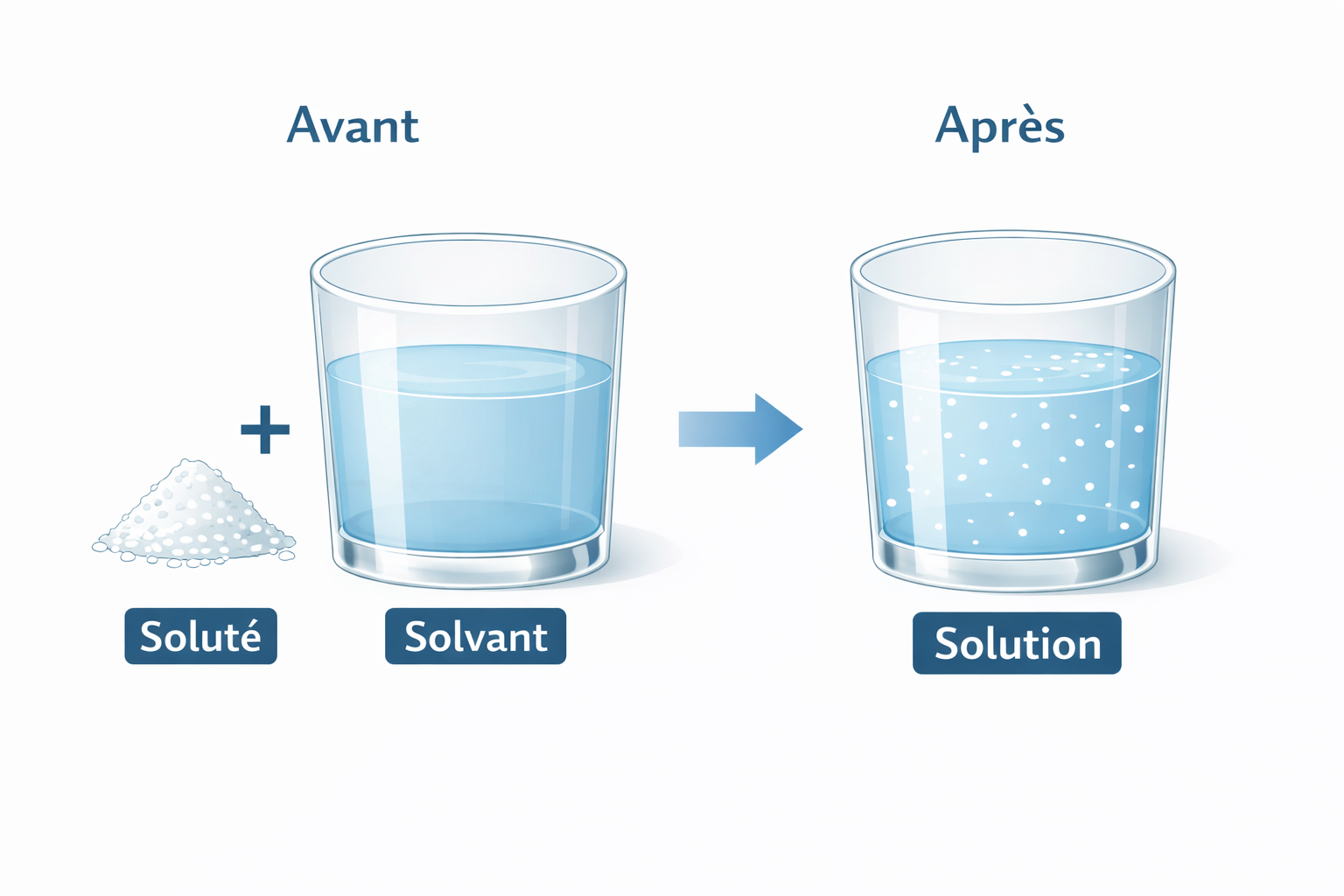
Solution
Une solution est un mélange homogène où le soluté est réparti de façon uniforme dans le solvant.
On ne peut pas dissoudre une quantité infinie de soluté : quand le solvant ne peut plus dissoudre, on obtient une solution saturée (le soluté en excès reste visible).
Le sel dissous dans l’eau forme une solution saline.
| Terme | Rôle | Exemple |
|---|---|---|
| Soluté | Substance dissoute | Sel (NaCl) |
| Solvant | Liquide qui dissout | Eau |
| Solution | Mélange homogène obtenu | Eau salée |
- La dissolution permet de former des solutions, qui sont des mélanges homogènes.
- Une solution peut devenir saturée si on ajoute trop de soluté.
Partie 4 : Séparer les composants d’un mélange

Selon la nature des substances, différentes méthodes permettent de séparer les constituants :
- Filtration : séparer un solide non dissous d’un liquide (ex. : sable et eau).
- Sédimentation / décantation : laisser déposer un solide plus dense, puis verser le liquide clair ; ou séparer deux liquides non miscibles (ex. : eau et huile).
- Évaporation : récupérer un soluté dissous en éliminant le solvant (ex. : cristaux de sel à partir d’eau salée).
Si on veut récupérer aussi le solvant (par exemple de l’eau pure), on peut utiliser une autre technique : la distillation (niveau plus avancé).
| Méthode | Utilisation | Exemple |
|---|---|---|
| Filtration | Séparer solide non dissous / liquide | Sable et eau |
| Sédimentation / décantation | Séparer des phases (solide déposé ou liquides non miscibles) | Boue et eau ; eau et huile |
| Évaporation | Séparer soluté dissous et solvant (on récupère le soluté) | Sel et eau salée |
- Des méthodes physiques (filtration, décantation, évaporation) permettent de séparer les composants selon leurs propriétés.
Un mélange est constitué de plusieurs substances qui peuvent être visibles ou non. Les mélanges peuvent être homogènes (solutions) ou hétérogènes (plusieurs phases). La dissolution forme des solutions et peut conduire à une solution saturée si on ajoute trop de soluté. Pour séparer les composants d’un mélange, on utilise des méthodes physiques comme la filtration, la décantation ou l’évaporation.