Structure de l’atome
Problématique — Comment est constitué un atome, la plus petite unité d’un élément chimique ?
Comment est constitué un atome, la plus petite unité d’un élément chimique ?
- Connaître les principales parties de l’atome : noyau et électrons.
- Comprendre la composition du noyau : protons et neutrons.
- Savoir que les électrons se trouvent autour du noyau en couches électroniques.
- Relier le nombre de protons à l’identité de l’élément chimique.
Partie 1 : Qu’est-ce qu’un atome ?
Un atome est la plus petite partie d’un élément chimique qui conserve ses propriétés. Il est extrêmement petit et invisible à l’œil nu.
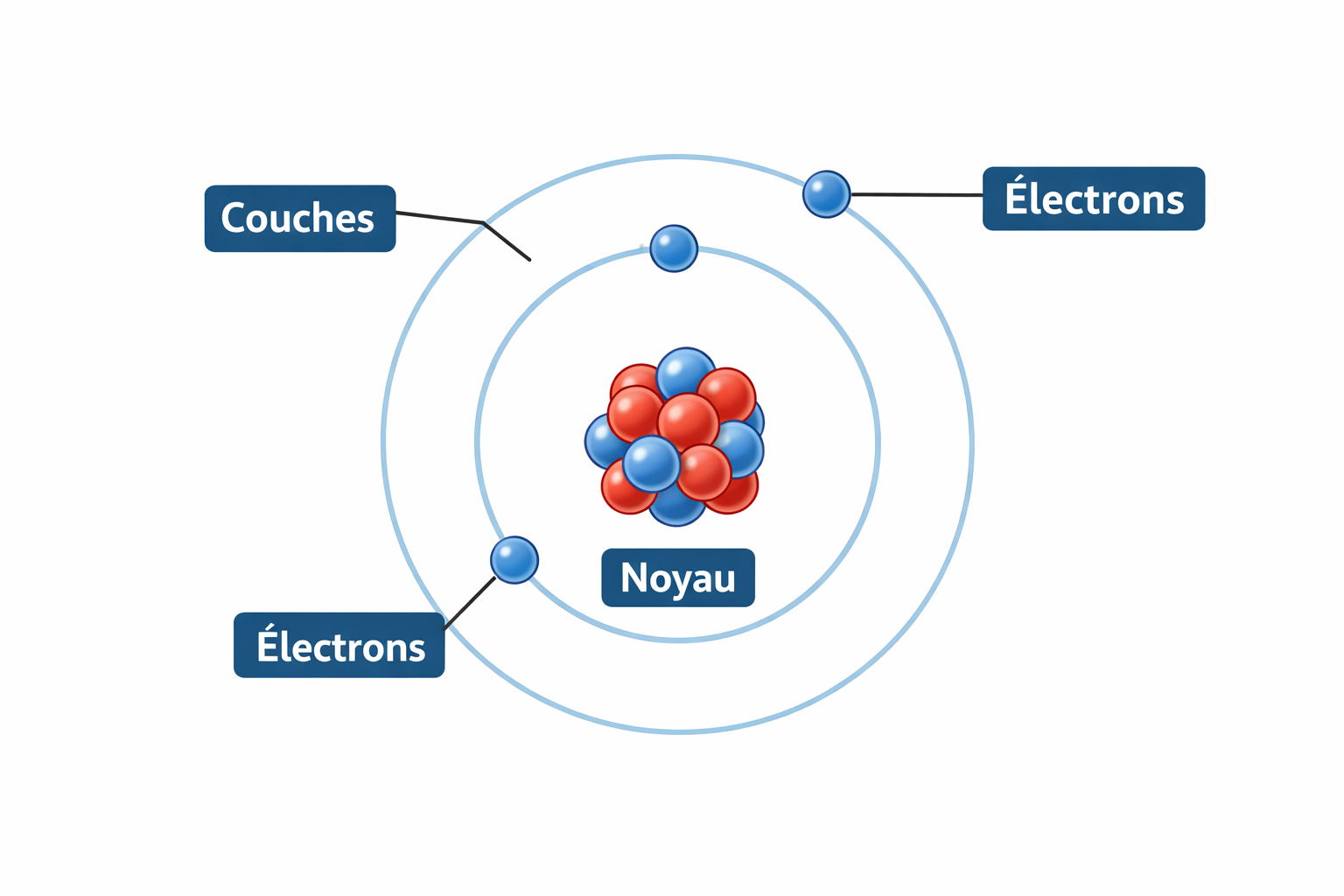
L’atome est constitué d’un noyau central et d’électrons qui se déplacent autour du noyau, dans des zones appelées couches électroniques.
| Notion | Idée clé |
|---|---|
| Atome | Plus petite unité d’un élément chimique conservant ses propriétés |
| Constitution générale | Noyau central + électrons autour (couches électroniques) |
- L’atome est constitué d’un noyau et d’électrons.
- Un atome correspond à un élément chimique (ex. : atome de carbone, d’oxygène…).
Partie 2 : Le noyau de l’atome
Le noyau est la partie centrale de l’atome.
Il contient des particules appelées protons (chargés positivement) et neutrons (sans charge).
Le nombre de protons détermine l’élément chimique : c’est le numéro atomique, noté Z.
- Z (numéro atomique) = nombre de protons.
- A (nombre de masse) = nombre de protons + neutrons.
- Donc : nombre de neutrons = A − Z.
| Particule | Charge | Rôle / Remarque |
|---|---|---|
| Proton | Positive | Son nombre (Z) détermine l’élément chimique |
| Neutron | Aucune (sans charge) | Avec les protons, il forme le noyau |
- Le noyau contient des protons (+) et des neutrons (0).
- Le nombre de protons (Z) définit l’identité de l’atome.
Partie 3 : Les électrons autour du noyau
Les électrons sont des particules chargées négativement.
Ils se déplacent autour du noyau et se répartissent dans des zones appelées couches électroniques.
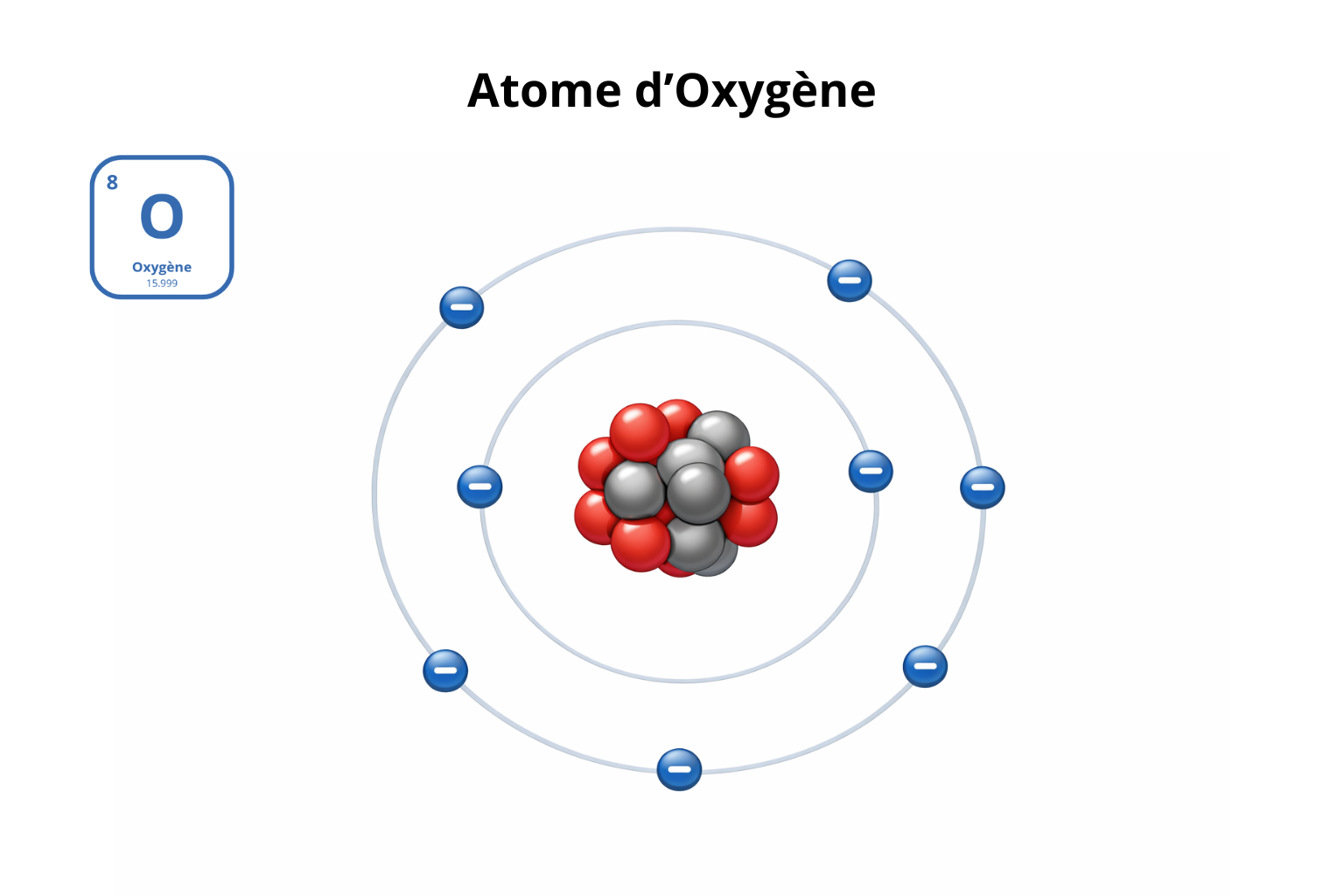
Dans un atome neutre, le nombre d’électrons est égal au nombre de protons.
Si un atome gagne ou perd des électrons, il devient un ion : il peut être chargé positivement (perte d’électrons) ou négativement (gain d’électrons).
| Notion | Idée clé |
|---|---|
| Électron | Particule chargée négativement |
| Couches électroniques | Zones où se répartissent les électrons autour du noyau |
| Atome neutre | Nombre d’électrons = nombre de protons |
- Les électrons (–) se répartissent autour du noyau en couches électroniques.
- Un atome est neutre si le nombre d’électrons égale le nombre de protons.
L’atome est constitué d’un noyau formé de protons (+) et de neutrons (0), entouré d’électrons (–) répartis en couches électroniques. Le nombre de protons (Z) définit l’élément chimique. Un atome neutre possède autant d’électrons que de protons ; s’il gagne ou perd des électrons, il devient un ion.